A terapia de RNA silencia o gene KRAS e aumenta o ataque imunológico às células cancerígenas

O bloqueio do KRAS e a ativação do sistema imunológico pela via RIG-I inflamam o microambiente do tumor, ajudando o corpo a combater melhor o câncer. Crédito: Trinh Tran, Departamento de Farmacologia, NUS Medicine
Dois estudos complementares liderados por investigadores da Escola de Medicina Yong Loo Lin, Universidade Nacional de Singapura (NUS Medicine), demonstraram uma nova estratégia terapêutica baseada em ARN que visa eficazmente um dos genes do cancro mais difíceis de tratar, o homólogo do oncogene viral do sarcoma de rato Kirsten (KRAS), ao mesmo tempo que estimula a resposta imunitária do corpo para combater tumores.
A pesquisa foi conduzida em amostras de células e modelos de laboratório, com colaboradores do Instituto NUS de Inovação e Tecnologia em Saúde (iHealthtech), Universidade Tecnológica de Nanyang (NTU), Agência de Ciência, Tecnologia e Pesquisa (A*STAR) e parceiros internacionais.
KRAS é um gene que atua como um interruptor molecular que controla como as células crescem e se dividem. Nas células saudáveis, esse interruptor liga e desliga conforme necessário. No entanto, em muitos tipos de câncer, incluindo câncer de pâncreas, pulmão e colorretal, o gene KRAS sofre mutação, travando o interruptor na posição “ligado”.
Esta ativação constante impulsiona o crescimento celular descontrolado e ajuda os tumores a escapar das defesas imunológicas normais. Mutações no KRAS estão entre as causas mais comuns de câncer humano e são encontradas em mais de 90% dos cânceres de pâncreas.
Como a proteína KRAS se liga firmemente às suas moléculas de sinalização e carece de locais de ligação fáceis de atingir, há muito que é considerada “indrogável” – tornando-a um dos alvos mais difíceis e importantes na investigação do cancro.
A equipe de pesquisa desenvolveu uma terapia combinada usando oligonucleotídeos antisense (ASOs) para silenciar genes KRAS mutantes e um RNA imunomodulador (immRNA) que ativa a via imunológica do gene I induzível por ácido retinóico (RIG-I).
A via RIG-I é semelhante a um sistema de alarme nas nossas células, onde detecta vírus e depois alerta o nosso sistema imunitário para lidar com a ameaça. Tanto os ASOs quanto as moléculas de imRNA foram entregues com segurança usando vesículas extracelulares derivadas de glóbulos vermelhos (RBCEVs), um transportador natural e biocompatível para medicamentos de ácido nucleico.
No primeiro estudo, publicado em Teranósticaos pesquisadores mostraram que o tratamento combinado ASO-imRNA matou células cancerígenas mutantes do KRAS – incluindo câncer de pulmão, colorretal e pancreático – bloqueando simultaneamente a atividade oncogênica do KRAS e desencadeando sinalização imunológica semelhante ao antiviral.
O tratamento duplo converteu tumores “frios” que normalmente evitam o ataque imunológico em tumores “quentes” que o sistema imunológico pode reconhecer e atacar, reduzindo a carga tumoral e prolongando a sobrevivência em estudos laboratoriais sem danificar as células normais.
Com base nesses resultados, o segundo estudo, publicado no Diário de liberação controladaavançaram a terapia para o estágio pré-clínico para câncer de pâncreas, principalmente adenocarcinoma ductal pancreático (PDAC), com metástase peritoneal.
PDAC é uma das formas mais mortais de câncer, com uma taxa de sobrevivência de cinco anos de 10%. No entanto, o tratamento suprimiu acentuadamente o crescimento do tumor, limitou a propagação abdominal e prolongou a sobrevivência em estudos laboratoriais. É importante ressaltar que os testes de segurança não mostraram toxicidade observável em estudos laboratoriais, apoiando o seu potencial para futuras avaliações clínicas.
“As mutações do KRAS sequestram as células cancerígenas e suprimem as respostas imunitárias, permitindo a metástase”, disse o Professor Associado Minh Le, Departamento de Farmacologia e Instituto de Medicina Digital (WisDM), NUS Medicine.
“Nossa plataforma EV visa precisamente mutantes, poupando tecidos saudáveis e sinergizando o KRAS knockdown com a ativação do RIG-I para liberar interferons, morte celular imunogênica e memória de células T – interrompendo o crescimento do tumor e estendendo a sobrevivência sem toxicidade.”
-

Mais morte de células cancerígenas (amarelo) é observada em minitumores pancreáticos (organoides) tratados com silenciamento combinado de KRAS e ativação de RIG-I em comparação com controles. Esquerda (verde): A laranja de acridina cora todas as células cancerígenas nos organoides para visualizar seu tamanho e estrutura. Meio (vermelho): O iodeto de propídio cora as células cuja integridade da membrana é perdida devido ao tratamento. Direita (mesclada): A sobreposição das duas manchas mostra células cancerígenas mortas (amarelo) dentro dos organoides. Crédito: Dai Phung, Departamento de Farmacologia, NUS Medicine
-

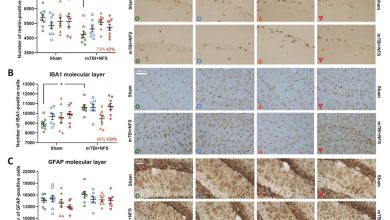
Mais células imunes migraram para os tumores pulmonares depois que um modelo de laboratório foi tratado com inibição combinada de KRAS e ativação RIG-I 1ª coluna: coloração H&E mostrando mais tumores (aglomerados densos de células com núcleos grandes e escuros) no tecido pulmonar do modelo não tratado. 2ª coluna: A análise de imagens H&E usando o software QuPath mostra menos tumores e mais células imunológicas (que ajudam a combater o câncer) nos pulmões dos modelos tratados em comparação com o grupo de controle. 3ª e 4ª colunas: Os modelos tratados mostram mais infiltração de duas principais células que combatem o cancro nos pulmões: células natural killer (NK) (castanhas, 3ª coluna) e células T citotóxicas (castanhas, 4ª coluna) em comparação com o grupo de controlo. A cor azul indica núcleos corados pela hematoxilina, permitindo a visualização de todas as células. Crédito: Dai Phung e Trinh Tran, Departamento de Farmacologia, NUS Medicine
O professor associado Glenn Bonney, consultor sênior da Divisão de Cirurgia Hepatobiliar e Pancreática do Departamento de Cirurgia do National University Hospital (NUH), que contribuiu com organoides derivados de pacientes para os estudos, acrescentou: “Esta entrega dupla de ácido nucleico por meio de vesículas biocompatíveis supera as barreiras de resistência do KRAS, oferecendo um caminho seguro e escalável para tratar metástases peritoneais – uma importante necessidade não atendida no PDAC”.
O professor Dahai Luo, da Escola de Medicina Lee Kong Chian da NTU e coautor dos artigos, acrescentou: “Ao projetar EVs para entrega direcionada, transformamos mensageiros celulares naturais em armas de precisão, com amplo potencial para outros tipos de câncer dependentes de KRAS, como colorretal e de pulmão”.
O professor adjunto Jonathan Loh Yuin-Han, vice-diretor executivo (pesquisa) do Instituto de Biologia Molecular e Celular (IMCB), A*STAR e coautor de uma publicação, disse: “Esta combinação inovadora de ASOs direcionados ao KRAS e agonistas RIG-I entregues por meio de vesículas extracelulares reprograma o microambiente tumoral, traçando um novo caminho para transformar os cânceres causados pelo KRAS e nos aproximando de imunoterapias eficazes e personalizadas com o potencial para salvar vidas e revolucionar o tratamento do câncer.”

Membros da equipe de pesquisa (da esquerda para a direita), Assoc Prof Minh Le, Rebecca, Gao Chang, Phuong Nguyen, Migara Jay, Dai Phung e Brendon Yeo. Crédito: Woon Fei e Alan, Departamento de Farmacologia, NUS Medicine.
A pesquisa destaca o potencial crescente das vesículas extracelulares como transportadores seguros e versáteis para terapias baseadas em ácidos nucleicos. Além do câncer de pâncreas, a plataforma pode ser adaptada a outras doenças malignas causadas pelo KRAS e combinada com imunoterapias existentes para melhorar os resultados do tratamento.
Mais informações:
Cao Dai Phung et al, A combinação de KRAS ASO e agonista RIG-I em vesículas extracelulares transforma o microambiente tumoral em direção ao tratamento eficaz de cânceres dependentes de KRAS, Teranóstica (2025). DOI: 10.7150/thno.105519
Tram TT Nguyen et al, Segurança e eficácia de oligonucleotídeos antisense KRAS e agonistas RIG-I entregues por vesículas extracelulares para tratamento de metástase peritoneal de câncer pancreático, Diário de liberação controlada (2025). DOI: 10.1016/j.jconrel.2025.114239
Fornecido pela Universidade Nacional de Singapura
Citação: A terapia de RNA silencia o gene KRAS e aumenta o ataque imunológico às células cancerosas (2025, 18 de novembro) recuperado em 18 de novembro de 2025 em https://medicalxpress.com/news/2025-11-discovery-rna-therapy-difficult-cancer.html
Este documento está sujeito a direitos autorais. Além de qualquer negociação justa para fins de estudo ou pesquisa privada, nenhuma parte pode ser reproduzida sem permissão por escrito. O conteúdo é fornecido apenas para fins informativos.