Estudo revela mecanismos epigenéticos que regulam a memória ILC2 e a recorrência da asma
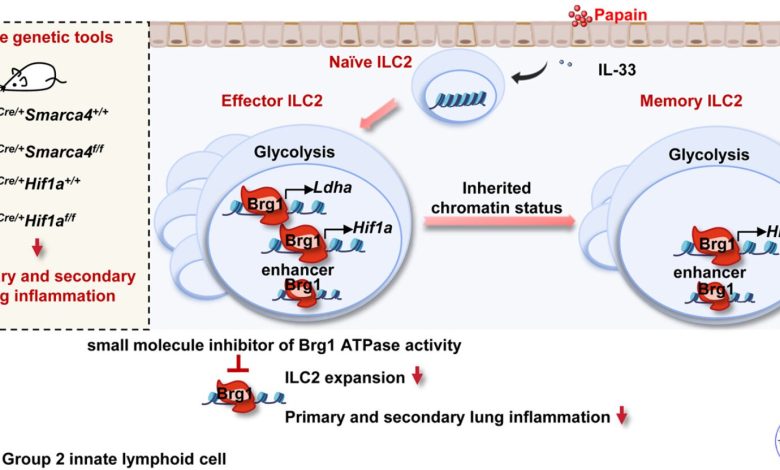

O status da cromatina impressa por Brg1 controla o metabolismo das células linfóides inatas do grupo efetor e de memória 2 para exacerbar a inflamação pulmonar alérgica. Crédito: Jornal de Alergia e Imunologia Clínica (2025). DOI: 10.1016/j.jaci.2025.08.029
Os pesquisadores revelaram um novo mecanismo pelo qual o gene 1 relacionado ao remodelador da cromatina brahma (Brg1) regula as células linfóides inatas do Grupo 2 (ILC2s) na inflamação pulmonar alérgica. Brg1 exacerba a inflamação pulmonar alérgica regulando o status da cromatina dos ILC2s, aumentando seu metabolismo glicolítico aeróbico e, consequentemente, promovendo a expansão dos ILC2s efetores (ILC2eff) e dos ILC2s de memória (ILC2mem).
Este estudo, liderado pelos Drs. Qiu Ju, Qin Jun e Qiu Jinxin do Instituto de Nutrição e Saúde de Xangai da Academia Chinesa de Ciências, foi publicado no Jornal de Alergia e Imunologia Clínica em 17 de setembro.
A asma é uma doença respiratória crônica em todo o mundo causada pela ativação excessiva da imunidade do tipo 2. Um tipo de célula imune inata denominada “ILC2s” desempenha um papel central neste processo, respondendo rapidamente a estímulos ambientais e induzindo diretamente a inflamação das vias aéreas. Após a exposição inicial ao alérgeno, os ILC2s podem entrar em um estado de “memória”. Após a reexposição a baixas doses do alérgeno ou a sinais inflamatórios (como IL-33), eles são rapidamente ativados e proliferam extensivamente, desencadeando uma “inflamação secundária” mais intensa. Esta é uma razão crucial pela qual a asma é recorrente e difícil de curar. No entanto, os mecanismos reguladores epigenéticos subjacentes que regem esta capacidade de memória permanecem obscuros.
Através de análises multiômicas, os pesquisadores descobriram que a expressão de Brg1 (codificado por Smarca4), um componente central do complexo de remodelação da cromatina mSWI/SNF, foi significativamente regulada positivamente em um modelo de inflamação pulmonar alérgica em camundongos. A citocina inflamatória IL-33, um sinal chave que induz a ativação de ILC2 na asma, induziu diretamente a expressão de Brg1 em ILC2s, sugerindo que Brg1 pode ser uma “chave chave” para a ativação de ILC2.
Outras experiências demonstraram que durante a ativação do ILC2, o Brg1 se liga e abre uma série de regiões da cromatina, particularmente loci genéticos relacionados ao metabolismo celular. Notavelmente, o Brg1 promove o processo glicolítico em ILC2s, aumentando a acessibilidade à cromatina dos principais genes metabólicos, como Hif1a e Ldha, apoiando assim a sua expansão e sobrevivência.
Os pesquisadores também descobriram que essa “impressão metabólica” moldada por Brg1 pode ser retida dos ILC2s efetores para os ILC2s de memória, permitindo que as células de memória mantenham altos níveis de atividade glicolítica e capacidade de resposta rápida após reexposição a alérgenos. Em modelos animais, o nocaute específico de Smarca4 ou Hif1a em ILC2s inibiu significativamente a proliferação de ILC2 e aliviou a inflamação pulmonar aguda e secundária, demonstrando que Hif1α é uma molécula chave que conecta Brg1 às características de memória de ILC2s.
Em relação à prática clínica, os pesquisadores intervieram ainda usando o composto 14, inibidor de Brg1 de molécula pequena. Eles descobriram que esse inibidor não apenas aliviou efetivamente a inflamação pulmonar alérgica em camundongos, mas também demonstrou eficácia superior em comparação aos esteróides tradicionais (dexametasona) na supressão da resposta de memória ILC2. Estas descobertas sugerem que atingir o Brg1 pode representar uma nova estratégia potencial para o tratamento da asma e outras doenças alérgicas.
Este estudo revelou o mecanismo epigenético pelo qual Brg1 imprime respostas efetoras e de memória ILC2 para exacerbar a asma primária e recorrente. Estas descobertas não só aprofundam a nossa compreensão da patogênese da asma, mas também fornecem novos insights sobre o desenvolvimento de novas terapias direcionadas à memória imunológica inata.
Mais informações:
Jupei Tang et al, o status da cromatina impressa por Brg1 controla o metabolismo das células linfóides inatas do grupo efetor e de memória 2 para exacerbar a inflamação alérgica pulmonar, Jornal de Alergia e Imunologia Clínica (2025). DOI: 10.1016/j.jaci.2025.08.029
Fornecido pela Academia Chinesa de Ciências
Citação: Estudo revela mecanismos epigenéticos que regulam a memória ILC2 e a recorrência da asma (2025, 23 de outubro) recuperado em 23 de outubro de 2025 em https://medicalxpress.com/news/2025-10-reveals-epigenetic-mechanisms-ilc2-memory.html
Este documento está sujeito a direitos autorais. Além de qualquer negociação justa para fins de estudo ou pesquisa privada, nenhuma parte pode ser reproduzida sem permissão por escrito. O conteúdo é fornecido apenas para fins informativos.


