Modelo evolutivo para resistência a antibióticos revela o tempo de dose crítico para os cuidados
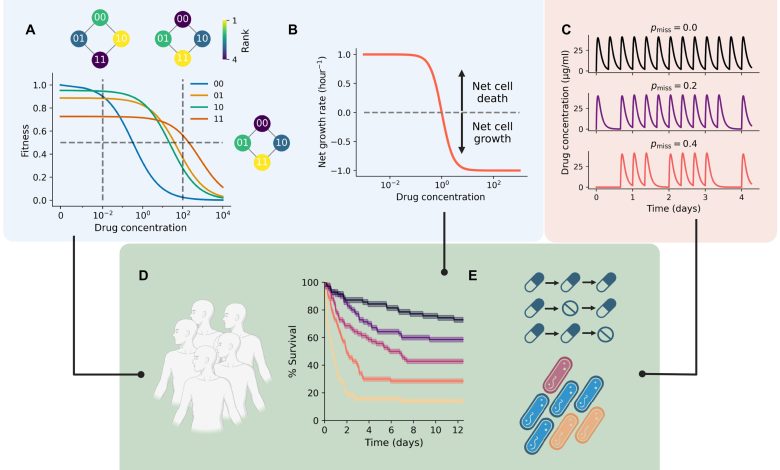

As paisagens marítimas de fitness modelam intrinsecamente as compensações evolutivas. Crédito: Avanços científicos (2025). Doi: 10.1126/sciadv.adv126
Os pesquisadores da Cleveland Clinic estão trabalhando para melhorar a maneira como usamos a modelagem evolutiva para entender a resistência a medicamentos. O estudo, publicado em Avanços científicosusa um novo tipo de modelo evolutivo chamado “paisagem marítima de fitness” para incorporar o cronograma de dosagem de um paciente em modelos que prevêem se uma infecção desenvolverá resistência a antibióticos e descobriu que o tempo inconsistente e a falta de doses precoces podem levar à falha do tratamento.
Uma equipe liderada por Jacob Scott, MD, DPhil., Incluindo o primeiro autor autor Eshan King, um MD/Ph.D. Aluno da Case Western Reserve University School of Medicine, está refinando modelos que determinam doses de antibióticos recomendados, incorporando a dinâmica evolutiva bacteriana.
“Com o surgimento de ‘superbuzas’ ou infecções bacterianas resistentes a antibióticos, o mundo está atingindo um ponto de crise”, diz o Dr. Scott, autor sênior do estudo. “Já vimos do MRSA o que pode acontecer se uma bactéria se tornar resistente a antibióticos. Precisamos resolver o problema antes que ela afete nossa capacidade de usar antibióticos em aspectos mais rotineiros dos cuidados médicos, como cirurgia ou parto”.
Os médicos normalmente usam diretrizes de empresas farmacêuticas para decidir as dosagens de medicamentos para seus pacientes. Essas diretrizes dependem de equações que descrevem como os antibióticos são absorvidos no corpo para calcular a menor dose efetiva que trata a doença, sem deixar a área doente evoluir uma mutação resistente a medicamentos. Sob a orientação do Dr. Scott, King tem expansão alguns desses modelos para refletir melhor como as mudanças na concentração de um medicamento em nossa corrente sanguínea afetam a resistência ao tratamento.
“Muitos modelos assumem que o ambiente em torno de uma área doente não muda, mas o ambiente de uma infecção é nosso próprio corpo. Isso nunca é verdadeiramente constante”, diz King. “Nosso manuscrito se baseia no trabalho anterior para explicar mudanças na concentração de medicamentos ao longo do tempo em nossos corpos”.
Modelos de paisagem marítima são equações que incluem variáveis que mudam com o tempo ou o espaço, como a concentração de drogas. Isso permite que investigadores como King estudem novos aspectos da resistência a antibióticos, como como o momento entre doses influencia os níveis de medicação em áreas doentes. King usou modelagem à marsa para simular os resultados de centenas de pacientes virtuais sendo tratados para infecções bacterianas com antibióticos IV e orais.
“Outros modelos têm concentração de medicamentos como entrada e desfecho evolutivo (resistência ao tratamento) como uma produção. Em vez de testar diferentes concentrações de medicamentos em pacientes separados, nosso modelo nos permite girar um mostrador para alterar as concentrações em um paciente ao longo do tempo para refletir melhor como nosso corpo processa doses de medicamentos”, explica o Dr. Scott.
Antes deste estudo, perder uma dose ou interromper o tratamento com antibióticos precocemente foi enfatizado como principal contribuinte para a resistência ao tratamento. King ficou surpreso ao encontrar pacientes simulados que desenvolveram resistência ao tratamento, tomando aproximadamente a mesma quantidade de medicamentos que aqueles que eliminaram com sucesso sua infecção.
Em vez da presença ou ausência de medicamentos, foi o momento das doses de medicação que diferiram entre esses dois grupos. A equipe descobriu que desaparecer ou chegar atrasado com doses iniciais desempenhou um papel maior no desenvolvimento da resistência a antibióticos do que perder ou chegar atrasado com uma dose posterior.
A equipe testou esses achados no laboratório, tratando bactérias com diferentes regimes de antibióticos. As bactérias que receberam todas as doses recomendadas no horário recomendado provavelmente desenvolverão resistência ao tratamento.
Da mesma forma, as bactérias que receberam adequadamente as doses iniciais, mas perdidas posteriores não desenvolveram resistência. Por outro lado, as bactérias que perderam doses precoces, mas foram tratadas adequadamente, evoluíram a resistência ao tratamento, destacando um mecanismo potencial de falha no tratamento em um paciente.
“Esses resultados estão moldando como vou aconselhar meus pacientes”, diz King. “Vou enfatizar que eles realmente precisam estar em cima de tomar seus antibióticos nos intervalos de tempo recomendados, especialmente no início. Se eles tomam a primeira dose e depois perder a segunda dose e depois tomar a terceira dose, isso pode não funcionar tão bem. Há uma maior probabilidade de que esse tratamento falhe e teremos que tentar outra coisa”.
Mais informações:
Eshan S. King et al. Avanços científicos (2025). Doi: 10.1126/sciadv.adv1268
Fornecido pela Cleveland Clinic
Citação: Modelo evolutivo para resistência a antibióticos revela o tempo de dose crítico para os cuidados (2025, 13 de junho) recuperado em 13 de junho de 2025 de https://medicalxpress.com/news/2025-06-evolutário-ntibiotic-rensistância-reveals-dose.html
Este documento está sujeito a direitos autorais. Além de qualquer negociação justa para fins de estudo ou pesquisa particular, nenhuma parte pode ser reproduzida sem a permissão por escrito. O conteúdo é fornecido apenas para fins de informação.