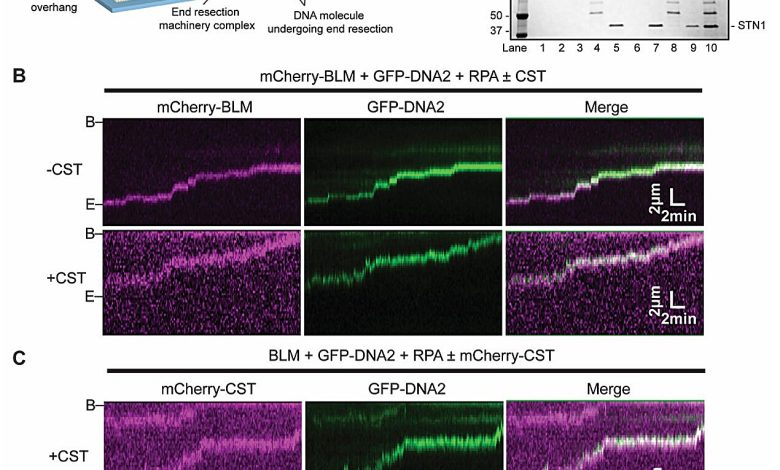
O complexo de DNA-chave conectado à resistência ao câncer de inibidor da polimerase descoberta

Análise de molécula única do CST-BLM-DNA2. Crédito: Ciência (2025). Doi: 10.1126/science.adt3034
Cientistas do Centro de Ciências da Saúde da Universidade do Texas em San Antonio (UT Health San Antonio) fizeram uma das descobertas mais importantes até o momento no estudo e tratamento de cânceres deficientes em BRCA1 e resistência a medicamentos.
Aproximadamente um em cada 300 americanos tem uma mutação patogênica no gene BRCA1 ou BRCA2, colocando -os em um risco elevado de desenvolver certos tipos de câncer, especialmente o câncer de mama e ovário. Dos que desenvolvem esses cânceres e são tratados com inibidores da PARP-uma terapia geralmente eficaz que tem como alvo poli (ADP-ribose) polimerases de que as células cancerígenas precisam de reparo e sobrevivência do DNA-a maioria dos pacientes eventualmente desenvolve resistência ao medicamento.
“Esta descoberta seminal abre a porta para entender como alguns cânceres de mama, próstata e ovário se tornam resistentes a uma classe importante de medicamentos cancerígenos chamados inibidores da PARP (polimerase). O complexo de reparo de DNA estudado no relatório é um alvo privilegiado para causar que a resistência e, portanto, é um novo alvo de terapia”, disse Robert Heras, Md, Md, FACP, e, portanto, é um novo alvo de terapia “, disse Robert Heras, Md, MD, e, portanto, é um novo alvo de terapia”, disse Robert Heras, Md, Md, e, portanto, é um novo alvo de terapia “, disse Robert Heras, Md, Md, e, portanto, é um novo alvo de terapia”. Medicina) na UT Health San Antonio.
Entendimento fundamental na resistência ao inibidor da PARP
O estudo, publicado em 22 de maio em Ciênciafoi co-liderado por Patrick Sung, Dphil, diretor do Instituto de Pesquisa do Câncer de Greehey Children e reitor associado de pesquisa na Long School of Medicine da UT Health San Antonio, e incluiu cientistas do Dana-Farber Cancer Institute da Harvard Medical School, Columbia University Irving Medical Center e UT Health Sanonio.
No estudo, eles explicam como a disfunção em um determinado complexo (complexo CST) que é crucial para regular como as quebras de DNA são reparadas podem levar à resistência ao inibidor da PARP em células cancerígenas deficientes em BRCA1.
“De todas as coisas que fizemos, essa tem mais impacto na prática clínica a longo prazo. Todo mundo espera que o mau funcionamento dessas proteínas dê origem à resistência a medicamentos, mas não sabem por que e como”, disse Sung.
O que é o complexo CST?
O complexo CST é composto de três proteínas e é um regulador negativo de um tipo de reparo de DNA chamado recombinação homóloga. Quando esse complexo está funcionando corretamente, os inibidores da PARP têm como alvo células cancerígenas deficientes em BRCA e fazem com que elas morram porque não podem reparar seu DNA. Como esse complexo proteico suprime a recombinação homóloga, se for mutada ou silenciada, as células tumorais podem se tornar resistentes aos inibidores da PARP e continuar a proliferação.
O primeiro autor Cody Rogers, Ph.D., bolsista de pesquisa de pós-doutorado do Instituto de Pesquisa de Câncer Infantil de Greehey na UT Health San Antonio, disse que o complexo CST é reconhecido principalmente como uma proteína de ligação ao DNA de fita única envolvida na regulação do comprimento dos telômeros. No entanto, ele disse, este estudo destaca as diferentes maneiras pelas quais o complexo CST trabalha para suprimir a recombinação homóloga e que as mutações nesse complexo causam resistência prontamente a inibidora de parp nas células deficientes em BRCA1.
“Existem dois mecanismos diferentes. Quando o CST restringe o EXO1, requer sua atividade de ligação ao DNA. Mas quando bloqueia a atividade do BLM-DNA2, ele age formando um complexo com BLM-DNA2 que não é funcional”, disse o co-primeiro Authoreep Kaur, Ph.D., Senior Research Scientist no Greehey Children Institute.
“Este é um primeiro passo crucial para fornecer uma estrutura intelectual para entender por que os defeitos nesse complexo em particular e outras proteínas associadas a esse complexo podem levar à resistência à droga ao câncer”, disse Sung.
“We are well-poised to provide a molecular explanation, and this will also form the basis of finding compounds that interfere with protein function or enhance the stability of DNA-bound protein complexes to boost the therapeutic efficacy of PARP inhibitors and other cancer drugs. Imagine if we could create a way to have CST stay on DNA longer and make BRCA1-deficient tumor cells super sensitive to different therapeutic agents. É um conceito provocativo. “
Mais informações:
Cody M. Rogers et al., CTC1-STN1-TEN1 Controla a escolha da via de reparo de quebra de DNA via bloqueio de ressecção final de DNA, Ciência (2025). Doi: 10.1126/science.adt3034
Fornecido pelo Centro de Ciências da Saúde da Universidade do Texas em San Antonio
Citação: O complexo de DNA-chave conectado à resistência ao câncer de inibidores da polimerase descoberta (2025, 10 de junho) recuperada em 10 de junho de 2025 de https://medicalxpress.com/news/2025-06-key-dna-clex-polymerase-inhibitor.html
Este documento está sujeito a direitos autorais. Além de qualquer negociação justa para fins de estudo ou pesquisa particular, nenhuma parte pode ser reproduzida sem a permissão por escrito. O conteúdo é fornecido apenas para fins de informação.

