Idade extrema protege contra câncer em estudo com ratos

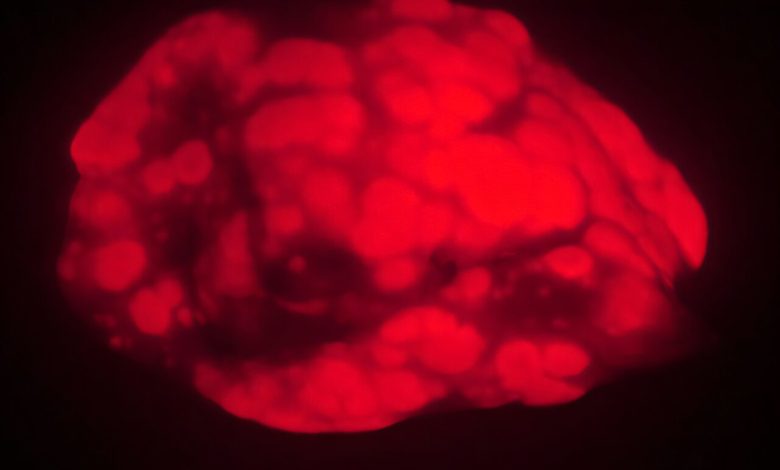
Camundongos velhos desenvolvem menos tumores pulmonares e menores (vermelho) do que animais mais jovens em um modelo de câncer. As descobertas sugerem que, em animais ou humanos muito idosos, o processo de envelhecimento suprime a formação de cancro. Crédito: Emily Shuldiner
Ratos de laboratório antigos desenvolvem substancialmente menos tumores pulmonares e menos agressivos do que animais mais jovens, num novo estudo liderado por investigadores da Universidade de Stanford. A descoberta vai contra o dogma estabelecido que afirma que o risco de cancro aumenta com a idade, mas enquadra-se com o que é observado em pessoas muito idosas, nas quais o risco de cancro parece estabilizar ou mesmo diminuir com a idade.
Monte Winslow, Ph.D., disse: “Esperávamos que os animais mais velhos tivessem mais e piores tipos de câncer, mas não foi isso que o estudo descobriu. Então, o que há nas mudanças moleculares associadas ao envelhecimento que suprimem o câncer?”
Apesar da intrigante sugestão de que o envelhecimento pode ter um lado positivo, tem sido difícil estudar o fenômeno completamente em laboratório. Na ausência de muitos dados, não foi possível saber como a idade de um paciente com câncer pode afetar sua capacidade de resposta às diversas opções de tratamento.
“O envelhecimento é uma mudança sistêmica no corpo, mas a maioria dos estudos sobre câncer em ratos são conduzidos em animais mais jovens”, disse a ex-aluna Emily Shuldiner, Ph.D. “Quando introduzimos as mesmas mutações causadoras de cancro do pulmão em ratos jovens e velhos, os ratos jovens desenvolveram mais tumores, de crescimento mais rápido”.
Shuldiner é o principal autor do estudo, publicado em Envelhecimento da Natureza. Os autores seniores do artigo são Winslow e o professor de biologia Dmitri Petrov, Ph.D.
Fatorando o fator idade
Faz sentido intuitivamente que o risco de câncer aumente com a idade. Cada vez que nossas células se dividem, há uma chance de atrapalhar a bola genética e introduzir mutações em nosso DNA que podem prejudicar a capacidade de uma célula de responder adequadamente a sinais que lhes dizem quando se dividir e quando se acalmar.
Durante a maior parte das nossas vidas, esse modelo parece ser verdadeiro: quando comparado com a idade, a incidência do cancro na população em geral aumenta acentuadamente a partir dos 50 anos e atinge o pico por volta dos 70 a 80 anos. Mas depois dos 85, a curva estagna e até cai.
Não está claro se essa mudança se deve a uma diminuição no rastreio e, portanto, no diagnóstico, ou talvez a uma espécie de seleção natural – talvez as pessoas predispostas à longevidade também tenham sistemas imunitários mais bem equipados para eliminar o desenvolvimento de cancros?
Mas os resultados nos ratos sugerem uma causa biológica mais profunda.
“O modelo padrão do câncer é que, com a idade, você acumula coisas ruins na forma de mutações”, disse Petrov, professor Michelle e Kevin Douglas na Escola de Humanidades e Ciências.
“E quando você coleta muitas coisas ruins, o câncer acontece. Depois de uma certa idade, deveria ser quase inevitável, certo? Mas não é isso que vemos; depois de um certo ponto, o envelhecimento parece ser uma forma genérica de supressão do câncer.”
Outras mudanças também se acumulam com a idade. Por exemplo, os padrões de etiquetas químicas no nosso ADN, chamados grupos metilo, que ajudam a regular quais os genes que são expressos e quando são expressos, são alterados. E o genoma geralmente se torna estruturalmente mais instável e vulnerável à quebra.
Segmentos de ADN nas fábricas de energia das nossas células podem duplicar-se e reintegrar-se no genoma, criando extensões de sequências repetidas, como vagões de carga idênticos numa linha de comboio.
No entanto, entre todo esse caos genético, algumas destas alterações prejudicam o desenvolvimento do cancro de uma forma que poderia ser explorada para novas terapias. Mas identificar isso em animais consome muito tempo.
Shuldiner abordou o problema de frente. Os ratos em seu estudo foram geneticamente modificados para desenvolver cânceres de pulmão marcados com fluorescência quando os animais foram tratados com um sistema de entrega de genes inalado. Mas para comparar a formação de tumores entre ratos jovens (quatro a seis meses) e velhos (20 a 21 meses), ela primeiro teve que esperar quase dois anos para que os animais envelhecessem. (A vida média de um rato de laboratório é de cerca de dois anos.)
Uma vez que os animais tinham dentes suficientemente longos, Shuldiner induziu a formação de câncer de pulmão. Quinze semanas depois, a quantidade de cancro nos pulmões dos ratos jovens – medida pelo peso pulmonar e imagens fluorescentes – era cerca de três vezes maior que a dos ratos mais velhos. Os ratos jovens também tinham cerca de três vezes mais tumores, e estes tumores eram significativamente maiores do que os encontrados em animais velhos.
“De todas as formas que pudemos medir, os animais mais jovens tiveram cancros piores”, disse Shuldiner.
Ela então investigou o efeito da inativação de 25 genes supressores de tumor nos animais antes de desencadear o desenvolvimento do câncer. Estes genes produzem proteínas que bloqueiam o desenvolvimento de cancros, e muitos estão envolvidos em processos associados ao envelhecimento normal.

scRNA-seq de células de pulmões portadores de tumor de KT jovens e idosos; H11LSL-Cas9 camundongos transduzidos com vetores Lenti-sgInert/Cre ou Lenti-sgPten/Cre. Para enriquecer as células cancerígenas, as suspensões unicelulares de pulmão inteiro foram divididas numa fracção de células cancerígenas e numa fracção a granel contendo todas as outras células vivas por triagem de células activadas por fluorescência (FACS). Crédito: Envelhecimento da Natureza (2025). DOI: 10.1038/s43587-025-00986-z
Quando é melhor ser velho
O impacto da inativação de qualquer um dos vários genes supressores de tumor foi diminuído em camundongos idosos. Isto é, embora a incidência tumoral tenha aumentado nos animais com supressores tumorais inativados, independentemente da idade, o efeito foi maior em camundongos mais jovens. Mas a inativação de um gene supressor de tumor em particular, o PTEN, teve um impacto muito maior do que os outros.
“A inativação do PTEN destacou-se por ter um efeito muito mais forte em ratos jovens”, disse Shuldiner. “Isso sugere que o efeito de qualquer mutação, ou a eficácia das terapias contra o câncer direcionadas a mutações específicas, pode ser diferente em pessoas jovens e idosas”.
Shuldiner também investigou os padrões de expressão genética em células cancerígenas de animais idosos com PTEN ativo ou inativo.
“Descobrimos que padrões conhecidos por estarem associados ao envelhecimento ainda estavam presentes nas células cancerígenas de ratos velhos”, disse Shuldiner.
“Esta não foi uma descoberta óbvia porque as células cancerígenas estão a dividir-se rapidamente. Foi interessante ver que essas assinaturas de envelhecimento permaneciam. No entanto, em animais velhos nos quais o PTEN foi inactivado, estas assinaturas de envelhecimento nas células cancerígenas eram muito menos pronunciadas. Pareciam tão jovens como as células cancerígenas deficientes em PTEN de animais jovens, o que foi muito surpreendente.”
O estudo é o primeiro a mostrar conclusivamente que o envelhecimento reprime a iniciação e o crescimento do tumor e que altera o impacto da inativação de genes supressores de tumor como o PTEN. Também descreve como as assinaturas do envelhecimento permanecem nas células cancerosas antigas, mesmo que estejam se dividindo rapidamente. As descobertas ilustram a importância do desenvolvimento de novos modelos celulares e animais de câncer que incorporem os efeitos do envelhecimento para desenvolver novas terapias.
“Desenvolvemos esses modelos animais de câncer com o objetivo de desenvolver novos tratamentos para os pacientes”, disse Winslow. “Mas para que isto funcione, os modelos têm de estar corretos. E este estudo sugere que os modelos que utilizam animais jovens podem não refletir com precisão alterações importantes relacionadas com o envelhecimento.”
“As implicações desta história podem ser enormes”, disse Petrov. “Talvez o envelhecimento tenha um lado benéfico que poderíamos aproveitar para melhores terapias”.
Mais informações:
Emily G. Shuldiner et al, O envelhecimento reprime a tumorigênese pulmonar oncogênica induzida pelo KRAS e altera a supressão tumoral, Envelhecimento da Natureza (2025). DOI: 10.1038/s43587-025-00986-z
Fornecido pelo Centro Médico da Universidade de Stanford
Citação: A idade extrema protege contra o câncer em estudo com ratos (2025, 13 de novembro) recuperado em 13 de novembro de 2025 em https://medicalxpress.com/news/2025-11-extreme-age-cancer-mouse.html
Este documento está sujeito a direitos autorais. Além de qualquer negociação justa para fins de estudo ou pesquisa privada, nenhuma parte pode ser reproduzida sem permissão por escrito. O conteúdo é fornecido apenas para fins informativos.



