Por que o transporte de energia no coração falha na cardiomiopatia hipertrófica

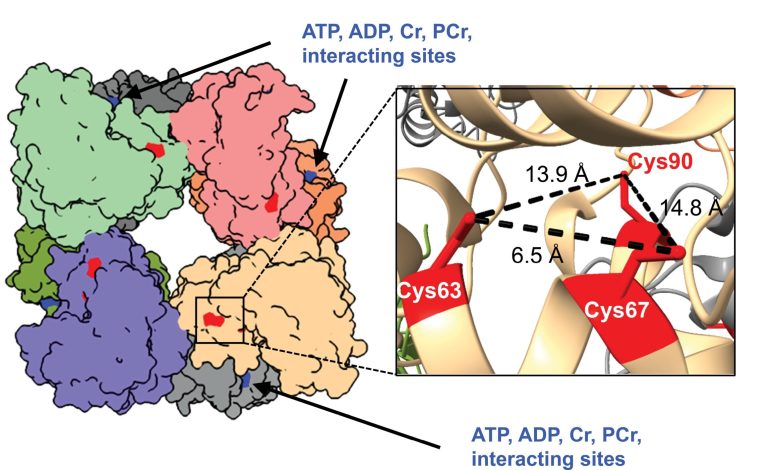
Como é construída a “lançadeira energética” do coração. A imagem mostra a forma 3D da creatina quinase mitocondrial. Crédito: Anton Xu et al., Circulaçãooutubro de 2025
A cardiomiopatia hipertrófica (CMH) é a doença cardíaca hereditária mais comum. Faz com que o ventrículo esquerdo fique mais espesso, o músculo cardíaco se contraia com muita força e trabalhe demais. Esta tensão adicional exerce pressão sobre as centrais eléctricas das células, as mitocôndrias, e pode aumentar o risco de arritmias cardíacas perigosas. A creatina quinase desempenha um papel fundamental na manutenção do equilíbrio entre o consumo e a produção de energia (homeostase energética). Esta enzima ajuda o coração a reciclar energia rapidamente para que cada batimento cardíaco receba a energia de que necessita.
Uma equipe do Departamento de Pesquisa Translacional do Comprehensive Heart Failure Center Würzburg (CHFC) trabalhou com parceiros nacionais e internacionais para investigar o papel da creatina quinase na CMH. Suas descobertas foram publicadas na revista Circulação.
Fortes contrações cardíacas aumentam o peróxido de hidrogênio nas mitocôndrias – a creatina quinase é desligada
“Descobrimos que sobrecarregar o músculo cardíaco faz com que as mitocôndrias produzam mais peróxido de hidrogênio. Essa molécula reativa de oxigênio normalmente ocorre em pequenas quantidades como subproduto, mas muito dela pode estressar ou danificar as células ao longo do tempo. Na CMH, o estresse oxidativo desliga a creatina quinase em dois locais importantes: nos filamentos, onde a força muscular é gerada, e nas mitocôndrias, onde a energia é produzido”, explica Anton Xu, doutorando do CHFC e primeiro autor do estudo.
“Isso significa que quando a creatina quinase é desativada, o coração não consegue manter um suprimento constante de energia onde é mais necessário. Isso aumenta o risco de arritmia cardíaca e causa estresse adicional”.
Os inibidores da miosina reduzem as contrações e, assim, protegem a creatina quinase da inativação e previnem arritmias celulares
A equipe observou essas alterações em biópsias cardíacas de pacientes com CMH e confirmou tanto a causa quanto o efeito positivo de um inibidor de miosina em vários modelos laboratoriais. Os inibidores da miosina reduzem a interação entre as proteínas contráteis actina e miosina, o que ajuda o músculo cardíaco a relaxar melhor e a se contrair com menos força.
“Nos nossos estudos, observámos que sob o efeito do inibidor da miosina, os níveis de peróxido de hidrogénio diminuíram, a função da creatina quinase foi mantida e os ritmos cardíacos anormais foram reduzidos”, relata o Dr. Vasco Sequeira, último autor do estudo. “Nossas descobertas sugerem, portanto, que tratamentos que reduzem a carga de trabalho do coração e limitam o estresse oxidativo podem ajudar a restaurar o equilíbrio energético e melhorar os resultados do tratamento na CMH”.
Observando os motores da miosina no coração em tempo real durante cada batimento cardíaco
Na próxima etapa, a equipe se concentrará em uma forma avançada de cardiomiopatia: a cardiomiopatia hipertrófica obstrutiva (CMHO). Nesta doença, um estreitamento na via de saída do ventrículo esquerdo causa resistência adicional ao sangue que flui para fora do coração. Isto significa que o coração tem que trabalhar ainda mais a cada batida.
Juntamente com parceiros do Centro Nacional Cerebral e Cardiovascular de Osaka, os investigadores de Würzburg pretendem desenvolver modelos animais mais realistas. Usando um sistema de raios X de alta resolução especialmente modificado, eles serão capazes de observar os minúsculos motores de miosina do coração, ou seja, as máquinas moleculares responsáveis pela contração, em tempo real durante cada batimento cardíaco no Instituto Japonês de Pesquisa de Radiação Síncrotron Spring 8 em Harima.
“Isto dá-nos uma visão sem precedentes da intensidade com que o coração trabalha, batimento a batimento, e permite-nos investigar até que ponto os mais pequenos vasos sanguíneos abastecem o músculo cardíaco com sangue e com que eficiência as células produzem e transportam energia”, explica Sequeira com entusiasmo.
Desenvolvimento de métricas para identificar pacientes que se beneficiarão do tratamento
Para refletir melhor a realidade, a equipe também investigará o estresse metabólico, como os efeitos negativos de uma dieta rica em gordura. Posteriormente, eles também examinarão se a redução da tensão no músculo cardíaco relacionada à obstrução usando inibidores de miosina restaura o transporte de energia do coração, estabiliza seu suprimento de energia e reduz o risco de arritmia cardíaca.
“Nosso objetivo é desenvolver medidas simples que ajudem os médicos a identificar os pacientes com CMHO que têm maior probabilidade de se beneficiar desses tratamentos de alívio”, resume o Prof. Dr. Christoph Maack, Chefe de Pesquisa Translacional e Porta-Voz do CHFC.
Mais informações:
Anton Xu et al, Hipercontratilidade e estresse oxidativo impulsionam a disfunção da creatina quinase na cardiomiopatia hipertrófica, Circulação (2025). DOI: 10.1161/circulaçãoaha.125.074120
Fornecido pelo Hospital Universitário de Würzburg
Citação: Por que o transporte de energia no coração falha na cardiomiopatia hipertrófica (2025, 24 de outubro) recuperado em 24 de outubro de 2025 em https://medicalxpress.com/news/2025-10-energy-heart-hypertrophy-cardiomyopathy.html
Este documento está sujeito a direitos autorais. Além de qualquer negociação justa para fins de estudo ou pesquisa privada, nenhuma parte pode ser reproduzida sem permissão por escrito. O conteúdo é fornecido apenas para fins informativos.