Descobertas experimentais de medicamentos abrem caminho para ensaios clínicos visando a indescritível mudança de crescimento do câncer

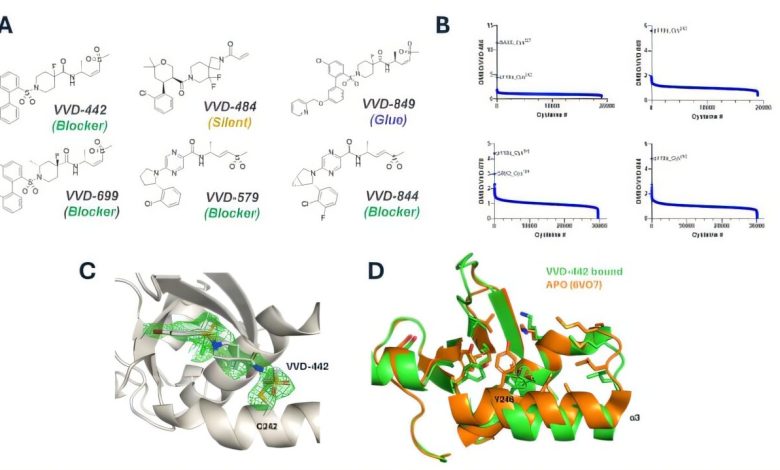
(A) Estrutura química dos ligantes VVD utilizados no manuscrito. (B) Seletividade proteômica global de VVD-484, VVD-849, VVD-579 e VVD-844. As células foram tratadas com 10 µM de VVD-484, 2 µM de VVD-849 ou VVD-579 ou 1 µM de VVD-844, que é ~25 vezes maior que TE50S. 20.000-30.000 peptídeos contendo cisteína foram medidos usando quantificação de TMT para cada composto. (C) FO-FC omite mapa contornado em 2,5 σ mostrando densidade contínua para VVD-442 e uma ligação covalente formada com Cys242. (D) Superposição do APO (PDB ID 6VO7) e domínio de ligação ao RAS ligado, destacando a mudança em α3 e o movimento de Tyr246 necessário para ligação de compostos. Crédito: Ciência (2025). DOI: 10.1126/science.adv2684
Pesquisadores do Francis Crick Institute e da Vividion Therapeutics identificaram compostos químicos que podem bloquear com precisão a interação entre o principal gene causador do câncer, RAS, e uma via chave para o crescimento do tumor.
Entrando agora no primeiro ensaio clínico em humanos, se forem considerados seguros e eficazes, estes medicamentos poderão ser usados para tratar muitos tipos diferentes de cancro, evitando ao mesmo tempo efeitos nas células saudáveis.
Um gene chamado RAS, que inicia as vias de crescimento celular, sofre mutação em cerca de um em cada cinco tipos de câncer. Versões mutadas do gene bloqueiam a proteína RAS num estado ativado, dizendo à célula cancerígena para continuar a crescer e a dividir-se.
A proteína RAS fica na membrana celular e é o primeiro “corredor” em uma retransmissão do crescimento celular. Mas bloquear completamente a actividade da proteína RAS ou das enzimas que ela controla pode causar efeitos secundários, porque estas vias de crescimento também são importantes para células saudáveis. Por exemplo, uma enzima que interage com o RAS, chamada PI3K, também interage com a insulina para controlar os níveis de açúcar, portanto bloqueá-la pode causar hiperglicemia.
Mas no seu trabalho, publicado hoje em Ciênciaa equipe de pesquisa usou uma combinação de triagem química e experimentos biológicos para encontrar e testar compostos que podem bloquear a interação entre RAS e PI3K sem causar efeitos colaterais em células saudáveis.
Cientistas da Vividion Therapeutics identificaram uma série de pequenos compostos que aderem irreversivelmente à superfície do PI3K perto do local de ligação do RAS e, em seguida, usando um ensaio desenvolvido pelos pesquisadores do Crick, descobriram que eles impediam a ligação do PI3K e do RAS, mas ainda permitiam que o PI3K interagisse com outras moléculas, como aquelas na via da insulina.
Pesquisadores do Laboratório de Biologia Oncogene de Crick e a equipe da Vividion testaram então um desses compostos em camundongos com tumores de pulmão com mutação RAS, descobrindo que o tratamento interrompeu o crescimento do tumor. É importante ressaltar que eles também verificaram e não observaram nenhuma evidência de hiperglicemia.
Eles então testaram o novo medicamento candidato em combinação com um ou dois outros medicamentos que também têm como alvo enzimas na via RAS. Esta combinação resultou numa supressão tumoral mais forte e duradoura em comparação com os tratamentos individuais isoladamente.
Finalmente, a equipe também testou o candidato a medicamento em camundongos com tumores contendo mutações em outro gene causador do câncer, o HER2. Este gene é frequentemente superexpresso no câncer de mama, e a proteína HER2 também interage com PI3K. Os investigadores observaram uma supressão semelhante do crescimento tumoral e, surpreendentemente, este efeito foi independente do RAS, sugerindo que o medicamento candidato pode funcionar para bloquear o crescimento de ainda mais tipos de tumores.
O medicamento entrou agora no primeiro ensaio clínico em humanos para testar a segurança e os efeitos colaterais em pessoas com mutações RAS e HER2. O ensaio também avaliará se o tratamento potencial é mais eficaz em combinação com outros medicamentos direcionados à EAR.
Julian Downward, líder do grupo principal do Laboratório de Biologia Oncogênica em Crick, disse: “Dado que o gene RAS sofre mutação em uma ampla gama de cânceres, temos explorado como impedi-lo de interagir com as vias de crescimento celular por muitos anos, mas os efeitos colaterais atrasaram o desenvolvimento de tratamentos.
“Nosso esforço colaborativo superou esse desafio, visando especificamente a interação PI3K e RAS, deixando o PI3K livre para se ligar a seus outros alvos. É emocionante ver o início desses ensaios clínicos, destacando o poder da compreensão da química e da biologia fundamental para chegar a algo com potencial para ajudar pessoas com câncer.”
“Esta descoberta é um grande exemplo de como novas abordagens de descoberta podem abrir formas completamente novas de combater o cancro”, disse Matt Patricelli, Ph.D., Diretor Científico da Vividion.
“Ao projetar moléculas que impedem a conexão do RAS e do PI3K, ao mesmo tempo em que permitem que os processos celulares saudáveis continuem, descobrimos uma maneira de bloquear seletivamente um sinal chave de crescimento do câncer. É incrivelmente gratificante ver essa ciência agora progredindo na clínica, onde tem o potencial de fazer uma diferença real para os pacientes.”
Mais informações:
Joseph E. Klebba et al, Inibidores covalentes do domínio de ligação PI3Kα RAS prejudicam o crescimento do tumor impulsionado por RAS e HER2, Ciência (2025). DOI: 10.1126/science.adv2684
Fornecido pelo Instituto Francis Crick
Citação: Descobertas experimentais de medicamentos abrem caminho para ensaios clínicos visando a indescritível mudança de crescimento do câncer (2025, 9 de outubro) recuperado em 9 de outubro de 2025 em https://medicalxpress.com/news/2025-10-experimental-drug-pave-clinical-trial.html
Este documento está sujeito a direitos autorais. Além de qualquer negociação justa para fins de estudo ou pesquisa privada, nenhuma parte pode ser reproduzida sem permissão por escrito. O conteúdo é fornecido apenas para fins informativos.

