Cérebros desenvolvidos em laboratório com todos os principais tipos de células apoiam pesquisas terapêuticas de próxima geração

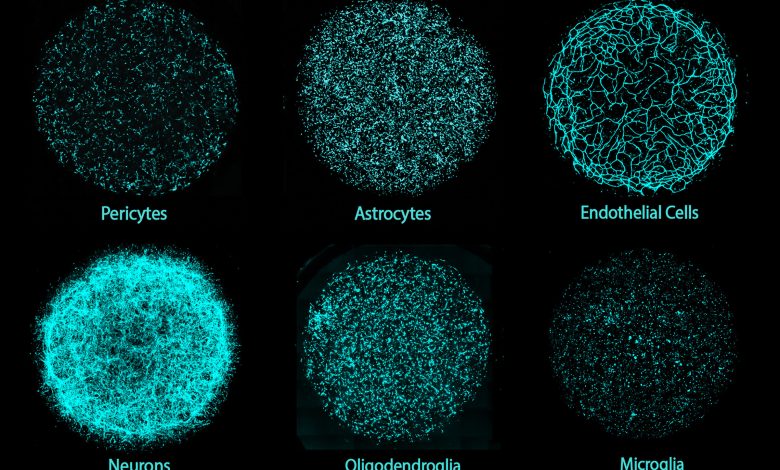
A coloração ciano mostra cada um dos seis principais tipos de células integrados em uma cultura miBrain. Crédito: Instituto MIT Picower/Instituto Koch
Uma nova plataforma 3D de tecido cerebral humano desenvolvida por pesquisadores do MIT é a primeira a integrar todos os principais tipos de células cerebrais, incluindo neurônios, células gliais e a vasculatura em uma única cultura. Cultivados a partir de células-tronco pluripotentes induzidas por doadores individuais, esses modelos – chamados de Cérebros Multicelulares Integrados (miBrains) – replicam características e funções importantes do tecido cerebral humano, são facilmente personalizáveis por meio de edição genética e podem ser produzidos em quantidades que apoiam pesquisas em larga escala.
Embora cada unidade seja menor que uma moeda de dez centavos, os miBrains podem valer muito para pesquisadores e desenvolvedores de medicamentos que precisam de modelos de laboratório vivos mais complexos para compreender melhor a biologia do cérebro e tratar doenças.
“O miBrain é o único sistema in vitro que contém todos os seis principais tipos de células presentes no cérebro humano”, disse Li-Huei Tsai, professor Picower, diretor do The Picower Professor of Learning and Memory e autor sênior do estudo que descreve o miBrains, publicado no Anais da Academia Nacional de Ciências.
“Na sua primeira aplicação, o miBrains permitiu-nos descobrir como um dos marcadores genéticos mais comuns para a doença de Alzheimer altera as interações das células para produzir patologia”, acrescentou.
Os co-autores seniores de Tsai são Robert Langer, professor do Instituto David H. Koch (1962), e Joel Blanchard, professor associado da Escola de Medicina Icahn no Monte. Sinai em Nova York e ex-pós-doutorado do Laboratório Tsai. O estudo é liderado por Alice Stanton, ex-pós-doutorado nos laboratórios Langer e Tsai e agora professora assistente na Harvard Medical School e no Massachusetts General Hospital, e Adele Bubnys, ex-pós-doutorado no laboratório Tsai e atual cientista sênior da Arbor Biotechnologies.
Benefícios de dois tipos de modelos
Quanto mais fielmente um modelo recapitular a complexidade do cérebro, mais adequado ele será para extrapolar como funciona a biologia humana e como possíveis terapias podem afetar os pacientes. No cérebro, os neurônios interagem entre si e com várias células auxiliares, todas dispostas em um ambiente tecidual tridimensional que inclui vasos sanguíneos e outros componentes. Todas essas interações são necessárias para a saúde e qualquer uma delas pode contribuir para doenças.
Culturas simples de apenas um ou alguns tipos de células podem ser criadas em quantidade com relativa facilidade e rapidez, mas não podem informar os pesquisadores sobre as inúmeras interações que são essenciais para a compreensão da saúde ou da doença. Os modelos animais incorporam a complexidade do cérebro, mas podem ser difíceis e caros de manter, lentos para produzir resultados e diferentes o suficiente dos humanos para produzir resultados ocasionalmente divergentes.
Os miBrains combinam vantagens de cada tipo de modelo, mantendo grande parte da acessibilidade e velocidade das linhas celulares cultivadas em laboratório, ao mesmo tempo que permitem aos investigadores obter resultados que refletem mais de perto a complexa biologia do tecido cerebral humano. Além disso, são derivados de pacientes individuais, tornando-os personalizados de acordo com o genoma de um indivíduo. No modelo, os seis tipos de células se auto-montam em unidades funcionais, incluindo vasos sanguíneos, defesas imunológicas e condução de sinais nervosos, entre outras características. Os pesquisadores garantiram que os miBrains também possuem uma barreira hematoencefálica capaz de controlar quais substâncias podem entrar no cérebro, incluindo a maioria dos medicamentos tradicionais.
“O miBrain é uma conquista científica muito interessante”, disse Langer. “Tendências recentes para minimizar o uso de modelos animais no desenvolvimento de medicamentos poderiam tornar sistemas como este ferramentas cada vez mais importantes para a descoberta e desenvolvimento de novos alvos de medicamentos humanos”.
Duas misturas ideais para modelos cerebrais funcionais
Projetar um modelo integrando tantos tipos de células apresentou desafios que exigiram muitos anos para serem superados. Entre as mais cruciais estava a identificação de um substrato capaz de fornecer estrutura física às células e apoiar a sua viabilidade. A equipe de pesquisa inspirou-se no ambiente que envolve as células do tecido natural, a matriz extracelular (MEC). A “neuromatriz” baseada em hidrogel do miBrain imita a MEC do cérebro com uma mistura personalizada de polissacarídeos, proteoglicanos e membrana basal que fornece uma estrutura para todos os principais tipos de células do cérebro, ao mesmo tempo que promove o desenvolvimento de neurônios funcionais.
Uma segunda mistura também seria crítica: a proporção de células que resultaria em unidades neurovasculares funcionais. As proporções reais dos tipos de células têm sido motivo de debate nas últimas décadas, mesmo com as metodologias mais avançadas fornecendo apenas pinceladas aproximadas para orientação, por exemplo, 45-75% para oligodendroglia de todas as células ou 19-40% para astrócitos.
Os pesquisadores desenvolveram os seis tipos de células a partir de células-tronco pluripotentes induzidas doadas por pacientes, verificando que cada tipo de célula cultivada recriava de perto células cerebrais que ocorrem naturalmente. Então, a equipe iterou experimentalmente até atingir um equilíbrio de tipos de células que resultou em unidades neurovasculares funcionais e adequadamente estruturadas. Este processo laborioso acabaria por ser uma característica vantajosa dos miBrains: como os tipos de células são cultivados separadamente, cada um deles pode ser editado geneticamente para que o modelo resultante seja adaptado para replicar estados específicos de saúde e doença.
“Seu design altamente modular diferencia o miBrain, oferecendo controle preciso sobre entradas celulares, antecedentes genéticos e sensores – recursos úteis para aplicações como modelagem de doenças e testes de drogas”, disse Stanton.
Descoberta de Alzheimer usando miBrain
Para testar as capacidades do miBrain, os investigadores iniciaram um estudo da variante genética APOE4, que é o mais forte preditor genético para o desenvolvimento da doença de Alzheimer. Embora se saiba que um tipo de célula cerebral, os astrócitos, é o produtor primário da proteína APOE, o papel que os astrócitos que transportam a variante APOE4 desempenham na patologia da doença é pouco compreendido.
Os miBrains foram adequados para a tarefa por dois motivos. Em primeiro lugar, integram os astrócitos com outros tipos de células do cérebro, para que as suas interacções naturais com outras células possam ser imitadas. Em segundo lugar, porque a plataforma permitiu à equipa integrar tipos de células individualmente, os astrócitos APOE4 poderiam ser estudados em culturas onde todos os outros tipos de células transportavam APOE3, uma variante genética que não aumenta o risco de Alzheimer. Isso permitiu aos pesquisadores isolar a contribuição dos astrócitos APOE4 para a patologia.
Em um experimento, os pesquisadores examinaram astrócitos APOE4 cultivados sozinhos, versus aqueles em miBrains APOE4. Eles descobriram que apenas nos miBrains os astrócitos expressavam muitas medidas de reatividade imunológica associada à doença de Alzheimer, sugerindo que o ambiente multicelular contribui para esse estado.
Os pesquisadores também rastrearam as proteínas amiloides e tau fosforiladas associadas ao Alzheimer, e descobriram que todos os miBrains APOE4 as acumularam, enquanto todos os miBrains APOE3 não o fizeram, como esperado. No entanto, em miBrains APOE3 com astrócitos APOE4, eles descobriram que os miBrains APOE4 ainda exibiam acúmulo de amiloide e tau.
Em seguida, a equipe investigou mais profundamente como as interações dos astrócitos APOE4 com outros tipos de células podem levar à sua contribuição para a patologia da doença. Estudos anteriores implicaram conversas cruzadas moleculares com as células imunológicas da microglia do cérebro. Notavelmente, quando os pesquisadores cultivaram miBrains APOE4 sem microglia, a produção de tau fosforilada foi significativamente reduzida. Quando os pesquisadores dosaram miBrains APOE4 com meios de cultura de astrócitos e micróglia combinados, a tau fosforilada aumentou, enquanto quando os dosaram com meios de culturas de astrócitos ou micróglia sozinhos, a produção de tau não aumentou. Os resultados forneceram, portanto, novas evidências de que a conversa cruzada molecular entre a micróglia e os astrócitos é de fato necessária para a patologia da tau fosforilada.
No futuro, a equipe de pesquisa planeja adicionar novos recursos ao miBrains para modelar mais de perto as características dos cérebros em funcionamento, como aproveitar a microfluídica para adicionar fluxo através dos vasos sanguíneos ou métodos de sequenciamento de RNA de célula única para melhorar o perfil dos neurônios.
Os pesquisadores esperam que o miBrains possa promover descobertas de pesquisas e modalidades de tratamento para a doença de Alzheimer e além.
“Dada a sua sofisticação e modularidade, existem direções futuras ilimitadas”, disse Stanton. “Entre eles, gostaríamos de aproveitá-lo para obter novos insights sobre alvos de doenças, leituras avançadas de eficácia terapêutica e otimização de veículos de distribuição de medicamentos”.
“Estou muito entusiasmado com a possibilidade de criar miBrains individualizados para diferentes indivíduos”, acrescentou Tsai. “Isso promete abrir caminho para o desenvolvimento da medicina personalizada.”
Mais informações:
Modelo de miBrain humano imuno-glial-neurovascular 3D projetado, Anais da Academia Nacional de Ciências (2025). DOI: 10.1073/pnas.2511596122
Fornecido pelo Instituto de Tecnologia de Massachusetts
Citação: Cérebros desenvolvidos em laboratório com todos os principais tipos de células apoiam a pesquisa terapêutica de próxima geração (2025, 18 de outubro) recuperado em 18 de outubro de 2025 em https://medicalxpress.com/news/2025-10-lab-grown-brains-major-cell.html
Este documento está sujeito a direitos autorais. Além de qualquer negociação justa para fins de estudo ou pesquisa privada, nenhuma parte pode ser reproduzida sem permissão por escrito. O conteúdo é fornecido apenas para fins informativos.

