O estresse agudo e crônico tem impactos marcadamente diferentes no reparo neural em uma região cerebral ligada à depressão

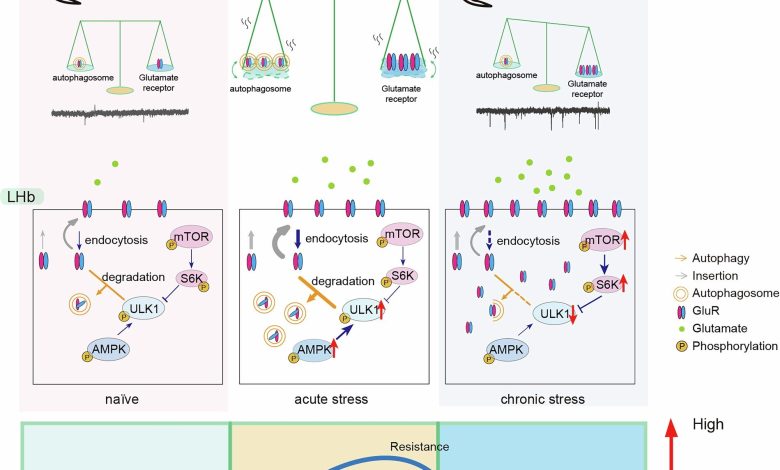
Modelo hipotético. Crédito: Natureza (2025). Doi: 10.1038/s41586-025-08807-4
Pesquisadores da Universidade de Zhejiang descobriram que o estresse agudo aumenta os mecanismos de reparo natural no cérebro, enquanto o estresse crônico os suprime. A autofagia foi mais afetada na habenula lateral, uma região do cérebro ligada à regulamentação emocional. Vários medicamentos antidepressivos foram testados e verificados para reverter essa supressão, apontando para a autofagia na habenula lateral como uma via terapêutica comum nesses tratamentos.
O transtorno depressivo maior afeta aproximadamente 10,6% das pessoas em todo o mundo e está entre as doenças psiquiátricas mais debilitantes. O estresse, um componente onipresente da vida cotidiana, tem sido identificado há muito tempo como um contribuinte importante para a depressão.
Embora o estresse moderado a curto prazo possa apoiar a sobrevivência, o estresse sustentado pode desestabilizar a regulação emocional. Como o cérebro se adapta ou falha em se adaptar no nível celular ao estresse permanece sem solução.
A autofagia, o processo celular de degradação e reciclagem de componentes internos, ganhou atenção crescente na neurociência. A autofagia regula a renovação de proteínas nos neurônios e tem sido implicada em condições neurológicas, como as doenças de Alzheimer e Parkinson. No entanto, o papel da autofagia nos distúrbios psiquiátricos relacionados ao estresse permanece incerto.
No estudo, “o estresse modula dinamicamente a autofagia neuronal para o início da depressão portador”, publicado em Naturezaos pesquisadores conduziram experimentos in vivo e in vitro para determinar se e como a autofagia na habenula lateral medeia os efeitos do estresse e dos antidepressivos.
As experiências foram realizadas em modelos de camundongos submetidos a várias formas de estresse agudo e crônico, incluindo restrição, derrota social e foco.
A atividade autofágica foi medida em várias regiões cerebrais usando técnicas como sequenciamento de RNA a granel, sequenciamento de RNA de núcle único, imunocoloração, microscopia eletrônica, análise de Western blot e teste comportamental. Os pesquisadores também usaram ferramentas genéticas para eliminar ou silenciar seletivamente genes relacionados à autofagia, incluindo ATG7, ATG5 e BECLIN-1, em regiões cerebrais específicas.
A administração sistêmica de antidepressivos, incluindo paroxetina, cetamina e rapamicina, foi usada para avaliar se esses tratamentos modularam a autofagia em animais expostos ao estresse. Os pesquisadores também infundiram diretamente um peptídeo ativador do Beclin-1 na habenula lateral para testar se o aumento da autofagia nessa região do cérebro poderia reverter comportamentos semelhantes à depressão.
O sequenciamento de RNA de seis regiões cerebrais relacionadas à emoção em camundongos estressados cronicamente mostrou que os genes relacionados à autofagia foram desregulados mais fortemente na habenula lateral de camundongos expostos ao estresse de restrição crônica. O sequenciamento de RNA único-nucleo confirmou que essa supressão ocorreu especificamente em neurônios.
Outras regiões cerebrais sensíveis ao estresse, incluindo o hipocampo ventral, a área tegmentar ventral e o córtex pré-frontal medial, não mostraram o mesmo padrão.
O estresse agudo aumentou os marcadores de autofagia na habenula lateral, conforme medido pelo aumento de LC3 Puncta, diminuiu os níveis de proteína p62 e maior contagem de autofagossomo sob microscopia eletrônica. O estresse crônico produziu o efeito oposto.
A análise de Western blot mostrou que a sinalização de mTOR elevada por estresse crônico, que é conhecido por inibir a autofagia, enquanto a sinalização AMPK ativada por estresse agudo, que a promove. Essas vias operam de forma independente.
O tratamento sistêmico com antidepressivos aumentou a atividade da autofagia na habenula lateral. Os marcadores de proteínas para autofagia melhoraram após o tratamento com paroxetina, cetamina ou rapamicina, mas permaneceram inalterados em oito outras regiões do cérebro. O bloqueio da autofagia com um inibidor seletivo negou os efeitos comportamentais dos antidepressivos e impediu a normalização da função sináptica.
Os ratos sem genes relacionados à autofagia na habenula lateral mostraram comportamentos semelhantes à depressão, incluindo aumento da imobilidade no teste de natação forçada e redução da interação social. O aumento da autofagia usando um peptídeo ativador do Beclin-1 reverteu esses comportamentos dentro de 30 minutos após o tratamento e manteve efeitos por até sete dias. Infusão do peptídeo durante a exposição ao estresse crônico também impediu o início de comportamentos semelhantes à depressão.
A análise de proteínas revelou que o estresse crônico levou a um acúmulo de subunidades do receptor de glutamato na habenula lateral. Esses receptores foram seletivamente degradados quando a autofagia foi restaurada.
Os registros de atividade sináptica mostraram que o aumento da autofagia reduziu a transmissão excitatória e os padrões de disparo neuronal normalizado nessa região. A endocitose do receptor de bloqueio eliminou esses efeitos. A autofagia parecia ser ativada “sob demanda” em neurônios altamente ativos.
Os autores concluíram que a autofagia na habenula lateral serve como um mecanismo celular que mantém a estabilidade emocional sob estresse, degradando receptores de glutamato excessivos. O estresse agudo ativa esse sistema através da sinalização da AMPK, enquanto o estresse crônico o desliga através da ativação do mTOR.
A interrupção da autofagia nessa região contribui diretamente para comportamentos semelhantes à depressão. Reestar a função autofágica, farmacologicamente ou geneticamente, foi suficiente para reverter ou prevenir esses efeitos.
Esses achados identificam a autofagia lateral da habenula como um guardião causal na transição do estresse para a depressão e um mecanismo compartilhado pelo qual múltiplos tratamentos antidepressivos exercem seus efeitos. O direcionamento desse processo pode levar a antidepressivos mais rápidos.
Mais informações:
Liang Yang et al. Natureza (2025). Doi: 10.1038/s41586-025-08807-4
Alberto Corona et al., O estresse crônico impulsiona a depressão, interrompendo a limpeza celular, Natureza (2025). Doi: 10.1038/d41586-025-00910-w
© 2025 Science X Network
Citação: O estresse agudo e crônico tem impactos marcadamente diferentes no reparo neural em uma região cerebral ligada à depressão (2025, 12 de abril) recuperada em 12 de abril de 2025 em https://medicalxpress.com/news/2025-04-acute-chronic-form-forms-nneur.html
Este documento está sujeito a direitos autorais. Além de qualquer negociação justa para fins de estudo ou pesquisa particular, nenhuma parte pode ser reproduzida sem a permissão por escrito. O conteúdo é fornecido apenas para fins de informação.