Mecânica da metástase do câncer de mama descoberta, oferecendo alvo para tratamento

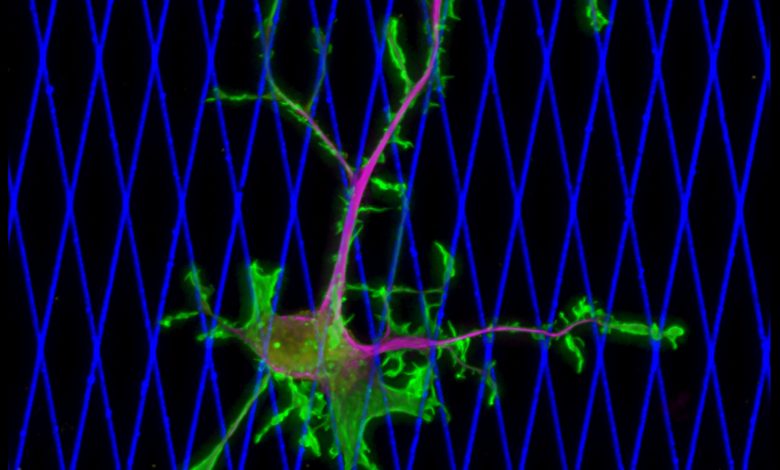
Uma célula de câncer de mama humano, o adenocarcinoma MDA-MB-231, demonstra adesão semelhante à metastática, espalhando-se e migrando em uma matriz de colágeno projetada para imitar tecidos moles. Uma nova pesquisa liderada pela Penn State revela pela primeira vez a mecânica por trás de como as células do câncer de mama podem invadir tecidos saudáveis. A descoberta, que mostra que uma proteína motora chamada dineína alimenta o movimento das células cancerígenas em modelos de tecidos moles, oferece novos alvos clínicos contra a metástase e tem o potencial de mudar fundamentalmente a forma como o cancro é tratado. Crédito: Erdem Tabdanov
A característica mais letal de qualquer câncer é a metástase, a disseminação de células cancerígenas por todo o corpo. Uma nova pesquisa liderada pela Penn State revela pela primeira vez a mecânica por trás de como as células do câncer de mama podem invadir tecidos saudáveis. A descoberta, que mostra que uma proteína motora chamada dineína alimenta o movimento das células cancerígenas em modelos de tecidos moles, oferece novos alvos clínicos contra a metástase e tem o potencial de mudar fundamentalmente a forma como o cancro é tratado.
“Esta descoberta marca uma mudança de paradigma em muitos aspectos”, disse Erdem Tabdanov, professor assistente de farmacologia na Penn State e principal co-autor correspondente do estudo, publicado recentemente na revista Ciência Avançada. “Até agora, a dineína nunca foi apanhada no negócio de fornecer a força mecânica para a motilidade das células cancerígenas, que é a sua capacidade de se moverem. Agora podemos ver que se você visar a dineína, poderá efetivamente interromper a motilidade dessas células e, portanto, pare a disseminação metastática.”
O projeto começou como uma colaboração entre o Departamento de Engenharia Química da Penn State e a Faculdade de Medicina da Penn State, antes de se transformar em uma parceria multi-institucional com pesquisadores do Centro Médico da Universidade de Rochester, do Instituto de Tecnologia da Geórgia, da Universidade Emory e da US Food e Administração de Medicamentos.
Os pesquisadores usaram microscopia ao vivo para observar a migração de células vivas de câncer de mama em dois sistemas diferentes modelados a partir do corpo humano. O primeiro sistema, uma rede bidimensional de fibras de colágeno, revelou como as células cancerígenas se movem através de uma matriz extracelular que envolve os tumores e mostrou que a dineína era a chave para o movimento das células cancerígenas. O segundo sistema foi um modelo tridimensional desenvolvido por uma equipe liderada por Amir Sheikhi, Dorothy Foehr Huck e J. Lloyd Huck Presidente de início de carreira em Biomateriais e Engenharia Regenerativa e professor assistente de engenharia química e engenharia biomédica na Penn State.
O segundo sistema foi projetado para imitar tecidos moles usando uma rede de partículas microscópicas de hidrogel ou microgéis ligadas entre si em formas semelhantes a tumores. Tal como no modelo bidimensional, os investigadores descobriram no modelo tridimensional que a dineína era “indispensável” na propagação ou metástase das células cancerígenas.
“Usando esses modelos tridimensionais que imitam parcialmente um tumor, descobrimos que, se bloquearmos a dineína, as células cancerígenas não poderão se mover e se infiltrar efetivamente nos tecidos sólidos”, disse Sheikhi. “Em ambos os modelos, descobrimos que a dineína é extremamente importante para a locomoção celular, o que sugere um método totalmente novo para o tratamento do cancro. Em vez de matar as células cancerígenas com radiação ou quimioterapia, estamos a mostrar como paralisá-las. Esta é uma óptima notícia porque você realmente não precisa matar as células, o que é uma abordagem severa que atinge tanto as células cancerosas quanto as saudáveis. Em vez disso, você apenas precisa impedir que as células cancerosas se movam.”
Tabdanov explicou que a “paralisia” celular poderia revelar-se uma estratégia de tratamento eficaz para o cancro em comparação com os tratamentos quimioterapêuticos, porque após a remoção cirúrgica do tumor principal, poderia impedir a propagação do cancro sem danificar tecidos e células saudáveis.
“O truque da quimioterapia é matar as células cancerígenas um pouco mais rápido do que o resto do corpo – é uma corrida contra o tempo”, disse Tabdanov. “A quimioterapia causa muitos danos aos tecidos normais e saudáveis do corpo enquanto está ocupada matando o câncer. Se, em vez disso, contivessemos o câncer e parássemos seu curso, poderíamos manter saudáveis as partes saudáveis do corpo.”
Os investigadores observaram que qualquer tratamento clínico potencial ainda está longe – uma vez que ainda não foram realizados ensaios em humanos ou animais. Sheikhi registrou diversas patentes relacionadas à plataforma de sua equipe e planeja usar a tecnologia para estudar uma infinidade de doenças, incluindo outros tipos de câncer.
“Estamos muito entusiasmados com esta colaboração com a Penn State College of Medicine e nossos laboratórios estão trabalhando em estreita colaboração em outros projetos”, disse Sheikhi. “Penso que estas plataformas poderão um dia permitir a medicina personalizada e o tratamento personalizado para o cancro e, esperançosamente, para muitas outras doenças.”
Outros autores do artigo são Yerbol Tagay, da Penn State College of Medicine; Sina Kheirabadi e Zaman Ataie, do Departamento de Engenharia Química da Penn State; Rakesh Singh, do Centro Médico da Universidade de Rochester; Denis Tsygankov, do Instituto de Tecnologia da Geórgia e da Universidade Emory; e Olivia Prince, Ashley Nguyen, Alexander Zhovmer e Xuefei Ma, da Food and Drug Administration dos EUA.
Mais Informações:
Yerbol Tagay et al, Dynein-Powered Cell Locomotion Guides Metastasis of Breast Cancer, Ciência Avançada (2023). DOI: 10.1002/advs.202302229
Fornecido pela Universidade Estadual da Pensilvânia
Citação: Mecânica da metástase do câncer de mama descoberta, oferecendo alvo para tratamento (2023, 27 de outubro) recuperada em 28 de outubro de 2023 em https://medicalxpress.com/news/2023-10-mechanics-breast-cancer-metastasis-treatment.html
Este documento está sujeito a direitos autorais. Além de qualquer negociação justa para fins de estudo ou pesquisa privada, nenhuma parte pode ser reproduzida sem permissão por escrito. O conteúdo é fornecido apenas para fins informativos.